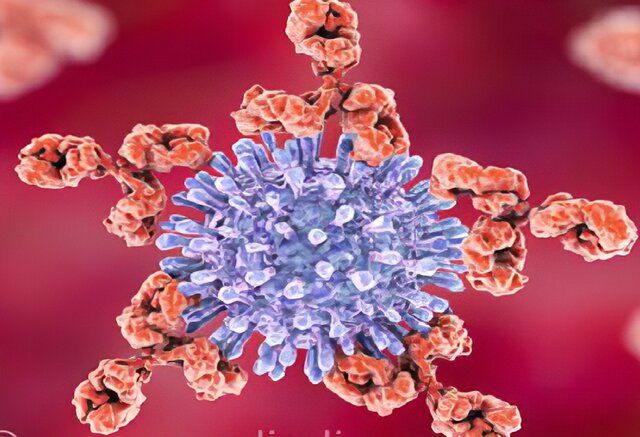
یک گروه بینالمللی از پژوهشگران در بررسی مشترکی، راهبرد جدیدی را کشف کردهاند که پادتنها به واسطه آن میتوانند جلوی ورود ویروسها به سلولهای بدن را بگیرند.
ساینسیو – به نقل از ایسنا و وبسایت رسمی دانشگاه پنسیلوانیا، این موضوع به طور گستردهای درک شده است که پادتنها، ویروسها را با چسبیدن به سطوح آنها خنثی میکنند و از توانایی آنها در آلوده کردن سلولهای میزبان جلوگیری میکنند اما یک پژوهش جدید نشان میدهد که این روش، تنها راهی نیست که پادتنها به واسطه آن، ویروسها را از کار میاندازند. یک گروه بینالمللی از پژوهشگران به سرپرستی “دانشگاه پنسیلوانیا”(Penn State) کشف کردهاند که پادتنها میتوانند ویروسها را منحرف کنند و در نتیجه، مانع اتصال و ورود درست آنها به سلولها شوند.
“گانش آناند”(Ganesh Anand)، استادیار شیمی دانشگاه پنسیلوانیا گفت: همه فکر میکنند که پادتنها به ویروسها متصل میشوند و مانع از ورود آنها به سلولها میشوند یعنی اساسا آنها را قفل میکنند اما پژوهش ما برای نخستین بار نشان میدهد که پادتنها ممکن است ویروسها را از نظر فیزیکی نیز منحرف کنند تا نتوانند به درستی به سلولهای میزبان متصل شوند و آنها را آلوده کنند.
آناند و همکارانش در این پژوهش، تعاملات میان یک “پادتن مونوکلونال انسانی”(HMAb) موسوم به “C10” و دو ویروس “زیکا”(Zika) و “دنگی”(Dengue) را بررسی کردند. پادتن C10 مورد استفاده در این پژوهش، پیشتر از بیماران مبتلا به ویروس دنگی به دست آمده بود که نشان داده بودند میتوانند ویروس زیکا را خنثی کنند.
پژوهشگران، ترکیبی از چند روش از جمله “میکروسکوپ الکترونی کرایو”(cryo-EM) را برای دیدن ویروسها و “طیفسنجی جرمی تبادل هیدروژن/دوتریوم”(HDXMS) را برای درک حرکت آنها به کار بردند.
آناند ادامه داد: میکروسکوپ الکترونی کرایو، محلول حاوی مولکولهای مورد نظر را بررسی میکند و سپس، آنها را با الکترونها هدف قرار میدهد تا تصاویر متعددی را از مولکولها در جهتهای گوناگون ارائه دهد. سپس، این تصاویر در یک عکس فوری از ظاهر مولکول ادغام میشوند. این روش، تصاویر بسیار دقیقتری از مولکولها را نسبت به سایر انواع میکروسکوپ ارائه میدهد.
پژوهشگران برای مستندسازی اثرات پادتنها روی ویروسهای زیکا و دنگی، عکسهای فوری میکروسکوپ الکترونی کرایو از ویروسها را در شرایط افزایش غلظت پادتنها جمعآوری کردند.
پژوهشگران در پروژه خود، از طیفسنجی جرمی تبادل هیدروژن/دوتریوم نیز استفاده کردند. در این روش، مولکولهای مورد نظر که در این پژوهش ویروس زیکا و دنگی بودند، همراه با پادتنهای مونوکلونال C10 در آب سنگین غوطهور میشوند. آناند توضیح داد که اتمهای هیدروژن آب سنگین، با دوتریوم جایگزین شدهاند که همزاد ایزوتوپی سنگینتر هیدروژن است.
وی افزود: هنگامی که یک ویروس در آب سنگین غوطهور میشود، اتمهای هیدروژن روی سطح ویروس با دوتریوم جایگزین میشوند. سپس میتوان از طیفسنجی جرمی برای سنجش سنگینی ویروس استفاده کرد. ما با انجام دادن این کار مشاهده کردیم که ویروس دنگی با دوتریوم، سنگینتر شد زیرا پادتنهای بیشتری به محلول اضافه شدند. این نشان میدهد که پادتنها ویروس دنگی را تحریف میکنند و اجازه میدهند دوتریوم بیشتری وارد آن شود. گویی ویروس در حال فشرده شدن است و سطح بیشتری در معرض دید قرار میگیرد که در آن میتوان هیدروژن را با دوتریوم مبادله کرد.
در مقابل، هنگامی که ویروس زیکا در آب سنگین قرار میگیرد، سنگینتر نمیشود و این نشان میدهد که اگرچه سطح آن کاملا توسط پادتنها اشغال شده اما توسط پادتنها منحرف نشده است.
آناند توضیح داد که این گروه پژوهشی با استفاده از میکروسکوپ الکترونی کرایو و طیفسنجی جرمی تبادل هیدروژن/دوتریوم توانستهاند تصویر جامعی را از آن چه هنگام چسبیدن پادتنها به ویروسهای زیکا و دنگی رخ میدهد، به دست آورند.
وی افزود: این کار مانند کتابهای مصور است که هر صفحه آن تصویر متفاوتی دارد و هنگامی که کتاب را ورق میزنید، یک فیلم کوتاه میبینید. یک کتاب با تصاویر اسب مسابقه را تصور کنید. میکروسکوپ الکترونی کرایو به شما نشان میدهد که اسب مسابقه چگونه به نظر میرسد و طیفسنجی جرمی تبادل هیدروژن/دوتریوم به شما سرعت حرکت اسب مسابقه را نشان میدهد. برای این که بتوانید یک اسب مسابقه را در حال حرکت توصیف کنید، به هر دو روش نیاز دارید. این مجموعه مکمل به ما کمک میکند تا بفهمیم چگونه یک نوع پادتن به طور متفاوت بر دو نوع ویروس تأثیر میگذارد.
آناند خاطرنشان کرد که این واقعیت که هرچه پادتنهای بیشتری اضافه شود، ذرات ویروس دنگی بیشتر منحرف میشوند، نشان میدهد که “قیاسسنجی” یا “استوکیومتری”(Stoichiometry) چقدر اهمیت دارد.
پژوهشگران دریافتند در شرایط اشباع که طی آن، پادتنها در غلظتهای کافی اضافه میشوند تا همه مکانهای اتصال موجود روی ویروسهای دنگی را پر کنند، ۶۰ درصد از ویروسها منحرف میشوند. این اعوجاج، برای محافظت از سلولها در برابر عفونت کافی بود.
آناند گفت: اگر پادتنها به قدر کافی وجود داشته باشند، ذره ویروس را به اندازه لازم منحرف میکنند تا پیش از رسیدن به سلولهای مورد نظر، بیثبات شوند.
زمانی که دانشمندان، ویروسهای دنگی متصل به پادتن را با سلولهای “BHK-21” در کلیه همسترهای نوزاد در تعامل قرار دادند، دریافتند که آلوده شدن سلولها، بین ۵۰ تا ۷۰ درصد کاهش یافته است.
آناند توضیح داد که پادتنها در برخی از ویروسها از جمله زیکا، با مسدود کردن راههای خروجی کار میکنند تا ویروس نتواند از آنها خارج شود.
وی افزود: ما مکانیسم جدیدی را در ویروس دنگی یافتیم که پادتنها به واسطه آن، راهها را میبندند تا ویروس نتواند بیرون بیاید.
پادتنها چگونه ذرات ویروس دنگی را منحرف میکنند؟
به گفته آناند، برخلاف “کروناویروس سندروم حاد تنفسی ۲”(SARS-CoV-2) که اکنون آشناست و دارای پروتئینهای خوشهای است که در همه جهات بیرون زدهاند، سطوح زیکا و دنگی صافتر هستند و برآمدگیهایی نیز دارند.
آناند خاطرنشان کرد که پادتنها در مورد ویروس دنگی، اتصال به برآمدگیهای موسوم به “رئوس پنجگانه”(five-fold vertices) را ترجیح میدهند. هنگامی که همه پروتئینهای رئوس پنجگانه متصل شوند، پادتنها به برآمدگیهای مورد نظر دوم خود یعنی “رئوس سهگانه”(three-fold vertices) روی میآورند. نهایتا، تنها “رئوس دوگانه”(two-fold vertices) باقی میمانند.
آناند اضافه کرد: پادتنها از رئوس دوگانه خوششان نمیآید زیرا بسیار متحرک هستند و اتصال به آنها دشوار است. ما متوجه شدیم هنگامی که رئوس پنجگانه و سهگانه به طور کامل به پادتنها متصل میشوند، اگر پادتنهای بیشتری را به محلول اضافه کنیم، ویروس شروع به لرزیدن میکند. این رقابت میان پادتنهایی که تلاش میکنند وارد شوند و ویروسی که تلاش میکند آنها را از بین ببرد، وجود دارد. در نتیجه، این پادتنها به جای اتصال به رئوس دوگانه، نهایتا به درون ویروس نفوذ میکنند. ما فکر میکنیم که این حفاری در ذره ویروس است که به تکان خوردن ویروس و از دست رفتن عملکرد آن منجر میشود.
تفاوت زیکا و دنگی چیست؟
آناند توضیح داد که زیکا یک ویروس بسیار پایدارتر و پویاتر از دنگی است که بخشهای متحرک زیادی دارد.
وی افزود: دنگی و زیکا شبیه به هم هستند اما هر کدام ویژگی متفاوتی دارند. دنگی ممکن است به عنوان یک ویروس متحرکتر، برای جلوگیری از گرفتار شدن توسط پادتنها تکامل یافته باشد. قسمتهای متحرک آن، سیستم ایمنی را گیج میکنند و از بین میبرند. پادتنها با نفوذ به ویروس دنگی و تحریف آن، راهی برای حل کردن این مشکل ایجاد کردهاند.
به گفته آناند، به نظر میرسد که یک نوع پادتن میتواند زیکا و دنگی را به دو روش متفاوت خنثی کند. یک روش، اتصال به ویروس و غیرفعال کردن آن است که روش سنتی در مورد فعالیت پادتن به شمار میرود و دیگری، نفوذ به ویروس و منحرف کردن آن است.
سایر ویروسها
آناند گفت: راهبردی که گروه او کشف کرده، ممکن است هنگام مواجهه با انواع دیگر ویروس نیز مورد استفاده پادتنها قرار بگیرد.
وی افزود: دنگی فقط یک ویروس نمونه است که ما در آزمایشهای خود از آن استفاده کردیم اما فکر میکنیم که این راهبرد پیشگیرانه ممکن است به صورت گسترده برای هر ویروسی قابل اجرا باشد. پادتنها ممکن است ابتدا به واسطه ایجاد یک سد، ویروسها را خنثی کنند و در صورت ناموفق بودن، به روش منحرف کردن متوسل شوند.
کاربردهای احتمالی یافتههای این پژوهش
آناند ادامه داد: شاید یافتههای این پژوهش برای طراحی پادتنهای درمانی، سودمند باشند. پادتنهای مونوکلونال C10، مخصوص ویروسهای دنگی و زیکا هستند و میتوانند این ویروسها را به دو روش گوناگون خنثی کنند اما شاید بتوان روشهایی را با همان قابلیتها برای درمان بیماریهای دیگر مانند کووید-۱۹ طراحی کرد. با ابداع یک دارو حاوی پادتنهایی که هم میتوانند راه ویروسها را مسدود سازند و هم آنها را منحرف کنند، احتمالا میتوانیم به خنثیسازی بیشتر دست پیدا کنیم.
وی افزود: هدف این نیست که منتظر بمانیم تا ویروس به بافت مورد نظر خود برسد؛ بنابراین اگر بتوان چنین درمانی را در قالب یک اسپری بینی ارائه داد، میتوان از ورود آن به سیستم ایمنی بدن جلوگیری کرد. با انجام دادن این کار، حتی ممکن است بتوان از پادتن کمتری استفاده کرد زیرا پژوهشهای ما نشان میدهند که برای خنثی کردن ویروس از طریق روش اعوجاج، پادتن کمتری مورد نیاز است.
اهمیت این پژوهش در این است که یک راهبرد کاملا جدید را نشان میدهد که برخی از پادتنها برای غیرفعال کردن برخی از ویروسها از آن استفاده میکنند.
آناند اضافه کرد: پیش از این، تنها چیزی که در مورد پادتنها میدانستیم، این بود که آنها به ویروسها متصل میشوند و آنها را خنثی میکنند. اکنون میدانیم که پادتنها میتوانند ویروسها را حداقل با دو روش گوناگون و شاید حتی بیشتر خنثی کنند. این پژوهش، دری را به روی یک مسیر کاملا جدید از اکتشافات باز میکند.
این پژوهش، در مجله “Cell” به چاپ رسید.